Резюме
Описаны наиболее часто встречаемые варианты патологии параартикулярных тканей (ППАТ) – энтезиты верхних и нижних конечностей, спины. Рассмотрены вопросы их этиологии, патогенеза, клиники, диагностики, дифференциальной диагностики.
Представлена история вопроса, техника проведения и механизм действия перифокальных шприцевых инъекций лекарственных препаратов.
Цель исследования: оценка клинической эффективности перифокальных шприцевых инъекций Алфлутопа у больных с энтезитами верхних и нижних конечностей и спины. Диагноз устанавливался клинически, а также по результатам рентгенологического обследования, данным УЗИ, МРТ.
Материалы и методы исследования: 76 больных с энтезитами плечевого сустава (30 пациентов), эпикондилитами (10), болями в спине (14), трохантеритами (13), анзеринитами коленных суставов (9) были пролечены перифокальными инъекциями Алфлутопа курсом по 5 инъекций с интервалом 1 инъекция в 2–3 дня. Оценивались общее самочувствие, локальная боль в покое, при пальпации и движении, объем движений.
Результаты лечения: получены хорошие результаты в виде улучшения самочувствия, уменьшения болей, увеличения объема движений. Значительное улучшение и улучшение отметили 69 пациентов из 76 – эффективность терапии составила 90,8% при хорошей переносимости препарата.
Ключевые слова: периартрит, патология параартикулярных тканей, энтезис, перифокальные инъекции, Алфлутоп
Для цитирования: Хитров Н.А. Лечение патологии параартикулярных тканей перифокальными инъекциями комбинированных препаратов.
Конфликт интересов: автор заявляет об отсутствии конфликта интересов.
Материалы и методы исследования
Одной из главных ценностей для современного человека является способность вести полноценную, независимую жизнь. Заболевания опорно-двигательного аппарата, причиняя механические, физические, психологические и эстетические страдания, ограничивают свободу человека. Сохранность органов движения является медицинской и социальной проблемой.
ПАТОЛОГИЯ ПАРААРТИКУЛЯРНЫХ ТКАНЕЙ
Большую часть заболеваний локомоторного аппарата составляют периартриты – патология параартикулярных тканей (ППАТ) суставов. ППАТ являются одной из самых частых жалоб со стороны взрослого населения. Среди первичных визитов к ревматологу обращения по поводу ППАТ составляют 59% [1]. Параартикулярные ткани представляют совокупность близких околосуставных структур и отдаленных от суставов тканей. Околосуставные ткани включают сухожилия мышц и их влагалища, сумки, связки, фасции, апоневрозы. Отдаленные от суставов структуры составляют мышцы, нервно-сосудистые образования, подкожно-жировая клетчатка.
Среди ППАТ выделяют:
- теносиновит – воспаление сухожильного влагалища,
- тендинит – воспаление сухожилия,
- бурсит – воспаление синовиальной сумки,
- энтезопатию (энтезит) – воспаление энтезиса – места прикрепления сухожилия или связки к кости или суставной капсуле,
- капсулит – поражение капсулы сустава,
- фасциит, апоневрозит – поражение фасций и апоневрозов [2].
В отличие от поражения самих суставов для ППАТ характерно:
1) несоответствие между активными и пассивными движениями (обычно ограничены активные движения при нормальном объеме пассивных),
2) усиление боли при строго определенных движениях,
3) отсутствие припухлости самого сустава,
4) локальная припухлость в проекции пораженной структуры.
Несмотря на стойкий болевой синдром и нарушение функции, лабораторные и рентгенологические изменения практически отсутствуют.
Распознаванию ППАТ успешно способствуют особенности топической диагностики данных структур:
1) поверхностное, часто подкожное, расположение структур,
2) близость анатомических костных ориентиров,
3) визуализация поражения: припухлость, гиперемия и т. д.,
4) легкость пальпации,
5) возможность построения рисунка боли, включающего триггерные точки, зоны распространения боли и т.п.,
6) оценка объемов нарушения движений (контрактуры: болевые, механические, спастические и т.п.),
7) оценка боли в покое и при движении,
8) оценка активных и пассивных движений,
9) использование провокационных проб (Тинеля, Фаленаи др.).
Диагностика ППАТ основывается на наличии локальных изменений: болезненности, уплотнения, отека, гипертермии, гиперемии. При опросе часто выявляется связь возникновения боли с травмой или повторяющимся нагрузочным движением. Обычно боль провоцируется движениями в данном суставе и стихает в покое. Пассивные движения в суставе больного, выполняемые врачом, менее болезненны, чем активные, которые совершает сам пациент [3]. В распознавании ППАТ помогают рентгенологические, ультра звуковые исследования (УЗИ), магнитно-резонансная томография (МРТ), при которых дифференцируются ППАТ, а также наличие включений в них – жидкости и т. п. [4, 5].
Причины ППАТ можно разделить на первичные и вторичные.
К первичным причинам развития ППАТ относятся острая травма, хроническая травматизация, хроническая механическая перегрузка, часто повторяющиеся стереотипные движения в суставе, непрямая травма. Вторично ППАТ возникают на фоне различных заболеваний: патологии опорно-двигательного аппарата (ортопедические аномалии развития, артрозы, артриты, спондилоартриты, синдром дисплазии соединительной ткани, гипермобильности суставов), эндокринно-обменных нарушений (сахарный диабет, нарушения жирового, кальциевого обмена, гипотиреоз, гиповитаминоз), нейротрофических нарушений, сосудистых расстройств, гипериммунных реакций, беременности и т. п. [2, 3]. На фоне провоцирующих факторов, особенно механических перегрузок, часто происходят рецидивы и хронизация ППАТ, что заставляет больного обращаться к врачу и вынуждает проводить лечение.
В последние годы среди различных вариантов ППАТ все большее место занимают энтезопатии – патология энтезисов (ЭТ). Термином «энтезис» обозначают место прикрепления сухожилий, связок, апоневрозов или суставных капсул к кости. Термин «энтезопатия» используется в медицинской литературе с 60-х гг. XX в., изначально он был введен для характеристики первично дегенеративных изолированных изменений, возникающих в энтезисах вследствие перегрузки.
В ЭТ волокна сухожилия или связки, перед тем как перейти в костную структуру, становятся более компактными, затем хрящевыми и, наконец, кальцифицированными. Питание ЭТ происходит посредством анастомозов через оболочки сухожилий паратенона, перихондра или периоста. ЭТ является метаболически активной структурой и хорошо иннервирован. Именно область ЭТ становится слабым звеном в аппарате околосуставных тканей, где при чрезмерной нагрузке возникают микро- и макроскопические повреждения, приводящие в последующем к локальному воспалению [6, 7].
Воспаление играет важную роль как при энтезопатиях, так и при других ППАТ. Воспаление лежит в основе обострения, усиливает дегенерацию тканей. Воспаление в ЭТ не ограничивается соединительной тканью (например, тендинит или фиброзит). Отмечается также вовлечение в патологический процесс хряща и кости, что приводит к возникновению периостита, а в дальнейшем – к появлению эрозий кости [1, 6].
Фиброзно-хрящевой ЭТ наиболее широко распространен в отличие от фиброзного ЭТ и характеризуется:
- компактностью зоны прикрепления к кости,
- расположением преимущественно в области эпифизов и апофизов,
- присутствием фиброзной хрящевой ткани.
Клиника энтезопатии часто определяет клинику ППАТ и характеризуется ограничением объема движений, спонтанной болью, болью при определенных движениях, болезненностью при пальпации, возможной припухлостью в области поражения [7]. При рентгенологическом исследовании энтезопатии характеризуются кальцификацией, костным ремоделированием, эрозиями костей в местах прикрепления сухожилий и связок. УЗИ и МРТ при энтезопатиях выявляют отеки, повреждение, разволокнистость структур. Часто обнаруживаются параэнтезитный отек и гиперэхогенные включения: кровь, хрящевые и костные структуры [4, 5].
ЛОКАЛЬНАЯ ТЕРАПИЯ ПОРАЖЕНИЙ ПАРААРТИКУЛЯРНЫХ ТКАНЕЙ
Одним из ведущих методов лечения ППАТ является локальная терапия (ЛТ). Особенностями ЛТ являются:
1) максимальное воздействие на орган-мишень,
2) достижение максимальной концентрации лекарства в целевом органе, что уменьшает системно назначаемые средства и снижает токсическое действие препаратов на организм,
3) при ЛТ лечатся органы, которые определяют трудоспособность и качество жизни больного,
4) важно, что ЛТ не исключает, а может (и часто должна)проводиться вместе с системным лечением!
Одним из методов ЛТ явилось перифокальное инъекционное введение лекарственного препарата. Имеется в виду введение его не в морфологические структуры костно-сухожильно-связочного аппарата ЭТ, а околоочаговое введение. Возможно использование разведения вводимого лекарства анестетиками, дистиллированной водой, физиологическим раствором для лучшего распространения и пенетрации лечебного препарата в пораженных структурах. Технически процедура представляет собой инъекцию лекарства непосредственно вблизи ЭТ, когда игла, проходя мягкие параартикулярные структуры, останавливается вблизи ЭТ. Глубина укола иглы легко определяется предварительной пальпацией пораженного ЭТ и окружающих его мягких параартикулярных тканей.
Развитию методики перифокальных инъекций препаратов способствовала техника инъекций лекарственных средств с помощью игольно-струйного инъектора «ИСИ-1», предложенного М.В. Провоторовым и И.А. Ханиным в Воронеже в 1982 г. для лечения заболеваний легких1. Были получены хорошие результаты в лечении пациентов с пневмониями.
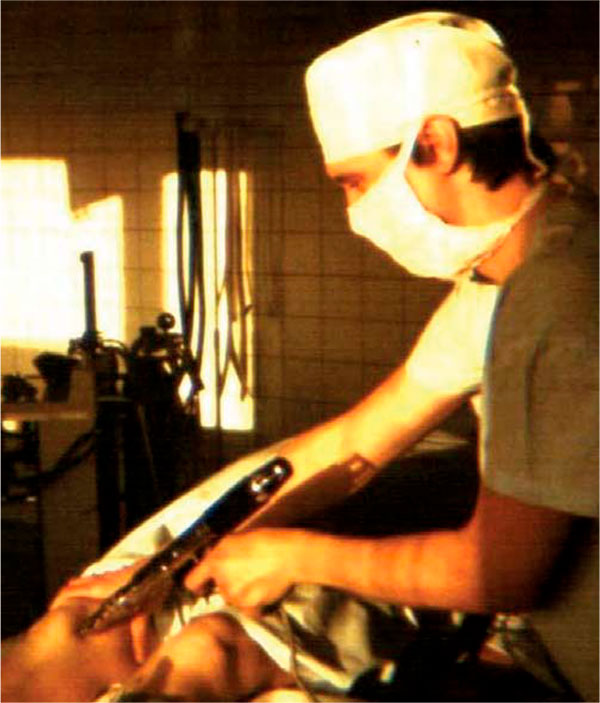
Рисунок 1. Техника выполнения игольно-струйной инъекции в коленный сустав с помощью аппарата «ИСИ-1»
Автор статьи с помощью аппарата «ИСИ-1» провел внутрисуставные инъекции 0,5 мл кеналога с 0,5 мл 2%-ного раствора новокаина для лечения 41 пациента с обострением остеоартрита коленного сустава и 14 больных с обострением ревматоидного артрита коленного сустава. После нажатия на спусковой крючок происходил быстрый (за 0,1 с) прокол мягких тканей иглой на 3–5 мм с последующим автоматическим струйным выбросом жидкого лекарственного препарата под давлением 200 кг/см2. Струя жидкости проходила через клетчатку, параартикулярные ткани, капсулу в полость сустава (рис. 1.). Полученные клинические результаты в виде уменьшения суставной боли, уменьшения припухлости сустава, увеличения объема движений в нем (эффективность лечения составила 90,2% у больных остеоартритом и 92,8% у больных ревматоидным артритом) позволили использовать в дальнейшем шприцевые перифокальные инъекции лекарств для лечения ППАТ.
Автором на секционном материале было показано проникновение большей части использованной для исследования метиленовой сини в полость коленного сустава с частичным параартикулярным (перифокальным) распространением вещества вокруг суставной капсулы, что, возможно, давало дополнительный лечебный эффект при инъекции лекарственного препарата2 (рис. 2).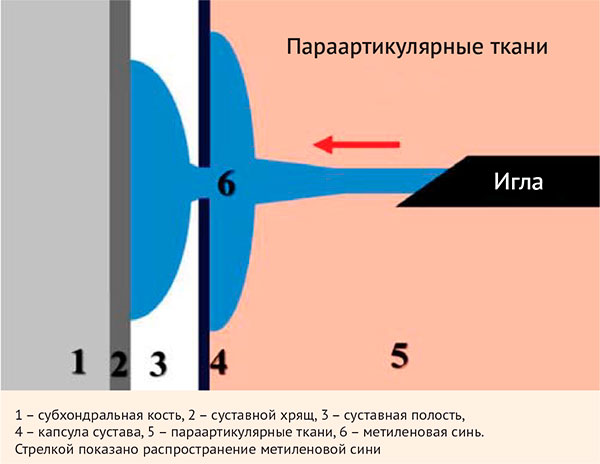
Рисунок 2. Схема интра- и параартикулярного распространения препарата при игольно-струйной инъекции аппаратом «ИСИ-1»
Так как ЭТ с прилегающей костной тканью является достаточно плотной анатомической структурой, то введение иглы в него затруднительно и травматично. Поэтому желательно довести иглу шприца до плотной анатомической структуры и вернуть обратно на 3–5 мм, после чего провести инъекцию лекарственного препарата. Суть перифокальной инъекции состоит в том, что лекарство оказывает лечебное действие, распространяясь вокруг фокуса поражения (перифокально) и проникая в него (рис. 3).
Положительными свойствами перифокальной инъекционной терапии являются локальность (прицельность, высокая местная концентрация, минимум системных побочных действий), отсутствие механического повреждения ЭТ, отсутствие проблем с развитием синовита и/ или инфекции, что актуально при сопутствующей суставной патологии.
АКЦЕНТЫ ЛЕЧЕНИЯ
Традиционно локальная инъекционная терапия ППАТ проводится с введением глюкокортикоидов (ГК). Но часто коморбидные состояния, например системный остеопороз, сахарный диабет, артериальная гипертензия, склонность ЖКТ к ульцерации на фоне ГК, локальные гипотрофические процессы и др., ограничивают применение инъекций ГК, особенно повторных, из-за высокой степени риска обострения сопутствующих заболеваний, развития асептического некроза костей, формирующих суставы, особенно головок плечевой и бедренных костей. Полярные представления о хондропротективных и хондродегенерирующих свойствах ГК имеют практически равное количество подтверждений. «При кортизонотерапии все, что мы делаем, это заменяем одно патологическое состояние другим», – писал C. Ragan. Местные анестетики: новокаин, лидокаин и т.п. – часто применяются при ППАТ, но действие их непродолжительное, и такое лечение не имеет патогенетической направленности [8, 9].
Так как в основе патоморфогенеза энтезитов лежат энтезитный «стресс», энтезитное воспаление и дегенеративная перестройка, то для лечения нужен лечебный препарат со структурно-модифицирующими и противовоспалительными свойствами. В качестве перифокальной инъекционной терапии применено курсовое местное шприцевое введение Алфлутопа – препарата с хондропротективными и противовоспалительными свойствами. Хондропротективный эффект Алфлутопа при его внутримышечном и внутрисуставном введении был доказан клинически и подтвержден данными МРТ [10, 11].
На основании двойного слепого плацебо-контролируемого рандомизированного многоцентрового исследования был доказан симптом-модифицирующий эффект Алфлутопа у 45 больных остеоартритом коленных суставов, получавших внутримышечные инъекции Алфлутопа по 1 мл курсами по 20 дней с 6-месячным интервалом в течение 2 лет, всего 4 курса за 2 года. В группе плацебо 45 пациентов получали инъекции изотонического раствора натрия хлорида по той же схеме. К концу исследования на фоне приема Алфлутопа отмечено достоверное снижение боли по сравнению с плацебо (p = 0,0003). Различия в абсолютной величине снижения интенсивности боли по WOMAC между группами оказались достоверными. Улучшение функции суставов, уменьшение суммарного индекса WOMAC были отмечены уже после первого курса терапии в группе Алфлутопа и сохранялись весь период наблюдения (р = 0,001). Достоверное улучшение качества жизни наблюдалось только в группе Алфлутопа (р = 0,0045). В группе, получавшей Алфлутоп, ответили на терапию 73% больных, в группе плацебо – 40% (р = 0,001). На фоне лечения Алфлутопом уменьшили суточную дозу нестероидных противовоспалительных препаратов (НПВП) 79% больных, а у 21% пациентов полностью отменили их прием. В группе плацебо снижение суточной потребности в НПВП наблюдалось только у 23% больных [12].
В данном же исследовании был доказан структурномодифицирующий эффект Алфлутопа. Рентгенологически подтверждено, что Алфлутоп замедлял прогрессирование остеоартрита коленных суставов: сдерживал сужение суставной щели и рост остеофитов, а также уменьшал деградацию матрикса суставного хряща. Достоверное замедление сужения суставной щели отмечено у больных, находившихся на терапии Алфлутопом, в отличие от больных, получавших плацебо. Увеличение размеров остеофитов наблюдалось у 72% больных, получающих плацебо, и только у 27% пациентов на фоне лечения Алфлутопом. Нарастание субхондрального остеосклероза тоже чаще определялось в группе получавших плацебо. Обнаружена тенденция к увеличению уровня маркера деградации хряща COMP в группе плацебо [13].
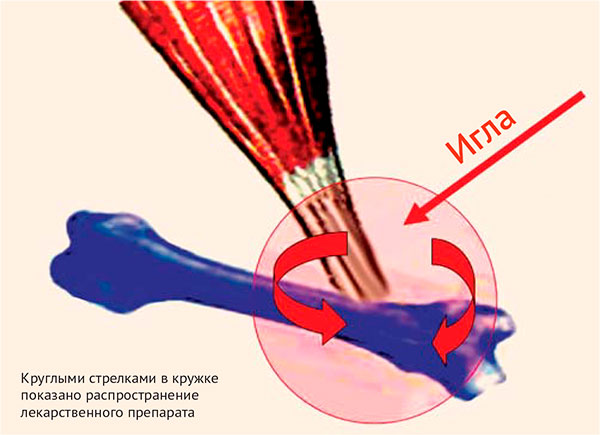
Рисунок 3. Схема перифокальной инъекции
В других работах были показаны следующие эффекты Алфлутопа. Реконститутивный и регенеративный эффекты: Алфлутоп стимулировал пролиферацию хондробластов на 53–64%, снижал активность гиалуронидазы на 83%, увеличивал экспрессию гиалуронан синтазы в 2,5 раза, стимулировал синтез аггрекана на 57%, снижал активность аггреканазы на 64%. Противовоспалительный эффект Алфлутопа состоял в уменьшении экспрессии генов провоспалительных цитокинов интерлейкина-6 и интерлейкина-8 при стимуляции воспаления в хрящевой ткани человека. В данной работе Алфлутоп также снижал высвобождение интерлейкина-8 на 45% и интерлейкина-6 на 24%. Антиоксидантный эффект характеризовался увеличением активности каталазы в 2,7 раза, уменьшением внутриклеточного супероксида аниона на 31% и пероксида водорода на 50% [14, 15].
Кроме того, в исследовании Дроздова В.Н. и соавт. показан дополнительный эффект Алфлутопа – гастропротективный, который связан с нормализацией синтеза простагландинов Е2 и F2а в слизистой оболочке желудка человека, нарушенного приемом НПВП при остеоартрите [16].
Алфлутоп производится из 4 видов морских рыб. В состав его входят гликозаминогликаны: хондроитин-6сульфат, хондроитин-4-сульфат, дерматансульфат, кератансульфат; глюкуроновая кислота; полипептиды, свободные аминокислоты; микроэлементы: Na, K, Fe, Са, Mg, Cu, Zn. Помимо терапии остеоартроза, Алфлутоп хорошо зарекомендовал себя в лечении сухожильно-связочного параартикулярного и паравертебрального аппарата [17, 18]. Хондропротективные, противовоспалительные и антиоксидантные свойства Алфлутопа побудили автора использовать его локально для лечения энтезопатий в области различных суставов и спины.
ЛЕЧЕНИЕ БОЛИ В ПЛЕЧЕ
ППАТ плечевой области – достаточно распространенное заболевание опорно-двигательного аппарата, которое встречается более чем у 10% больных, посещающих артролога или ревматолога. В основном это работающие люди в возрасте 40–60 лет. Заболевание одинаково поражает как мужчин, так и женщин.
Разнообразие форм ППАТ плеча связано с особенностями развитого параартикулярного аппарата плечевого сустава, осуществляющего самые различные движения: сгибание, разгибание, отведение, приведение, вращение и круговое движение. Движения в плечевом суставе обеспечивают мобильные функции руки и являются максимальными в сравнении с другими суставами человека. Из-за сложного параартикулярного аппарата и частоты ППАТ плечевой сустав называется периартритическим органом [19].
Большую часть ППАТ представляют теномиозиты мышц, составляющих так называемую манжету ротаторов плеча. Ротационная манжета формируется из четырех мышц: надостной, подостной, малой круглой и подлопаточной. При движении в плече ЭТ, связки, сухожилия и мышцы испытывают чрезмерную нагрузку, их волокна и сухожилия могут повреждаться, а в последующем развиваются воспалительные и дегенеративные процессы. Чаще всего поражаются ЭТ-дистальные отделы надостной и подлопаточной мышц в местах их прикрепления к большому и малому бугоркам плечевой кости соответственно.
Энтезопатии – повреждения с реактивным воспалительным компонентом ЭТ надостной и подлопаточной мышц – являются часто встречающимися формами ППАТ. Они имеют четкую клиническую картину, включающую затруднение движений, за которые отвечает данная мышца, и болезненность, усиливающуюся при пальпации ЭТ. При энтезопатии надостной мышцы больному трудно отводить и поднимать руку вверх во фронтальной плоскости. При пальпации плеча отмечается боль в верхнелатеральной части большого бугорка плечевой кости. При энтезопатии подлопаточной мышцы пациенту трудно завести руку за спину, при этом отмечается боль и локальная болезненность при пальпации в области малого бугорка плечевой кости [20].
Было проведено открытое исследование по эффективности и переносимости терапии Алфлутопом с участием 30 больных ППАТ плеча. Под критериями включения подразумевалось наличие у взрослых больных ППАТ в форме энтезопатий надостной и/или подлопаточной мышц, подтвержденных клинически. Всем больным проводилось рентгенологическое и ультразвуковое исследование пораженного сустава. Предусматривалась возможность амбулаторного наблюдения больного в период инъекций, понимание больным необходимости контакта с лечащим врачом и выполнения его предписаний.
Критериями исключения являлись беременность, наличие инфекционных заболеваний (системных, локальных, кожных), лихорадочные реакции, системные заболевания, меняющие метаболизм заживления раны (сахарный диабет, особенно 1-го типа, кахексия и т.п.), изменения в анализах крови воспалительного и/или метаболического характера, нарушения свертываемости крови, непереносимость новокаина.
В группу вошли 30 больных (12 мужчин, 18 женщин), средний возраст которых составил 51,3 ± 9,1 года, с длительностью заболевания от 1 до 14 месяцев. 17 пациентов страдали энтезопатией надостной мышцы и 13 пациентов – энтезопатией подлопаточной мышцы. У больных до начала лечения использовались нестероидные противовоспалительные препараты (НПВП), инъекции ГК, аппликационная терапия, физиолечение без положительного эффекта.
Больному за одну процедуру в 3 болевые точки, соответствующие анатомическому расположению ЭТ пораженных мышц, вводилось 2 мл Алфлутопа с 0,25%-ным раствором новокаина. Количество вводимого новокаина зависело от массы тела больного (рис. 4а, б, в).
Процедуру повторяли 2 раза в неделю, общее число – 5 инъекций. За период проведения инъекций другая терапия включала только соблюдение рекомендаций по режиму и прием НПВП в тех же лекарственных формах и в тех же дозировках, что и до лечения Алфлутопом.
На фоне курсового лечения Алфлутопом у большинства пациентов улучшилось самочувствие, что выражалось в повышении настроения, уменьшении раздражительности и нормализации сна, прежде всего за счет уменьшения приступов ночных болей. По окончании лечения Алфлутопом боли в плечевом суставе по визуально-аналоговой шкале (ВАШ) достоверно (р < 0,05) уменьшились с 67,2 ± 10,6 до 29,2 ± 5,8 мм. Объем движений в угловых градусах увеличился с 39,9 ± 6,8 до 142,6 ± 13,1. На фоне лечения инъекциями Алфлутопа пациенты снизили дозы принимаемых НПВП на 30–70%. По окончании лечения Алфлутопом значительное улучшение самочувствия (уменьшение боли более чем на 75%, отказ от обезболивающих препаратов) отмечено у 9 больных (оценка врача совпадала с оценкой пациента), улучшение (уменьшение боли на 25–75%, снижение приема обезболивающих препаратов) – у 17, отсутствие динамики – у 4. Отрицательной динамики не выявлено (рис. 5а, б, в)
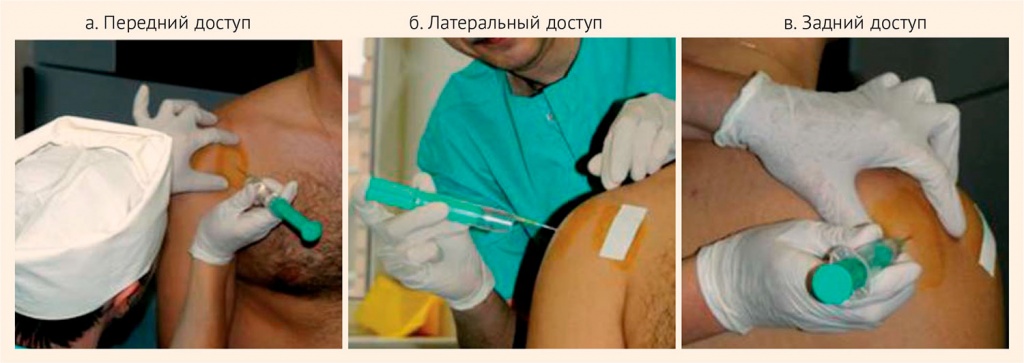
Рисунок 4. Методика перифокальных инъекций в параартикулярные ткани плечевого сустава
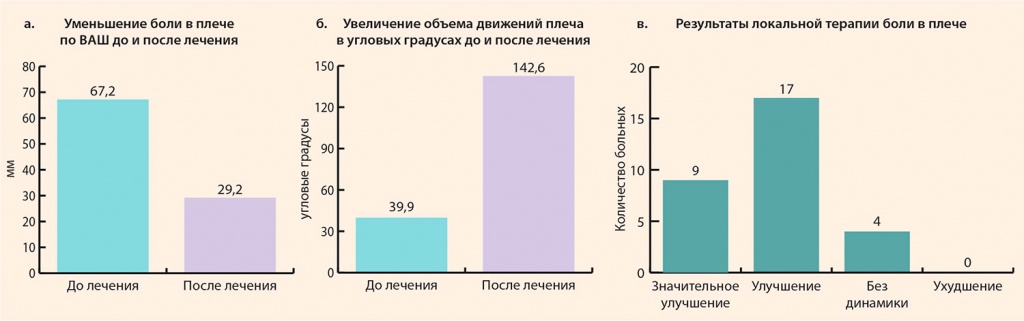
Рисунок 5. Динамика у пациентов с ППАТ плеча после курсового лечения Алфлутопом
ЛЕЧЕНИЕ ЛОКТЕВЫХ ЭПИКОНДИЛИТОВ
Среди ППАТ локтевого сустава часто встречаются эпикондилиты: наружный – «локоть теннисиста» (Tennis elbow) и внутренний – «локоть игрока в гольф» (Golfers elbow) [21]. Основной симптом эпикондилита — боль в области надмыщелка плечевой кости в покое, чаще при пальпации и усиливающаяся при ротационных движениях в локтевом суставе и движениях в кисти (сгибание и разгибание). Боль усиливается при пальпации, причем эпицентр боли может локализоваться, во-первых, в области надмыщелка плечевой кости – в местах ЭТ мышц предплечья, во-вторых, ниже надмыщелка – в области сухожилий прилегающих мышц. В-третьих, возможен эпицентр боли при пальпации в верхней трети предплечья – в местах прохождения самих мышц, что говорит о различной степени вовлечения в патологический процесс энтезисов, сухожилий и мышц у разных больных.
Наружный эпикондилит («локоть теннисиста») встречается чаще внутреннего эпикондилита. Появлению боли предшествует механическая усиленная или необычная нагрузка: работа на даче, занятия спортом после большого перерыва, ремонт и т. д. Пациент точно указывает место наибольшей болезненности, соответствующее наружному надмыщелку плечевой кости – ЭТ, где прикрепляются сухожилия разгибателей кисти и пальцев или проекции сухожилий данных мышц. Поэтому эпицентр боли может располагаться несколько ниже надмыщелка. Боль возникает при сопротивлении активному разгибанию в лучезапястном суставе, распространяется по наружной поверхности локтя при вращательных движениях (например, при работе с отверткой и т.п.). В точке максимальной болезненности могут отмечаться отек, покраснение и местное повышение температуры.
Внутренний эпикондилит («локоть игрока в гольф») представляет собой энтезопатию мышц – сгибателей кисти и пальцев, прикрепляющихся в области внутреннего надмыщелка плечевой кости. В этом месте определяется пальпаторная болезненность, боль также воспроизводится при сопротивлении активному сгибанию кисти в лучезапястном суставе. Часто пациент, страдающий эпикондилитом, сам показывает наиболее болезненные для него движения. При латеральном эпикондилите боли усиливаются при супинации предплечья и разгибании кисти, а при медиальном эпикондилите боли возникают и усиливаются при пронации предплечья и сгибании кисти.
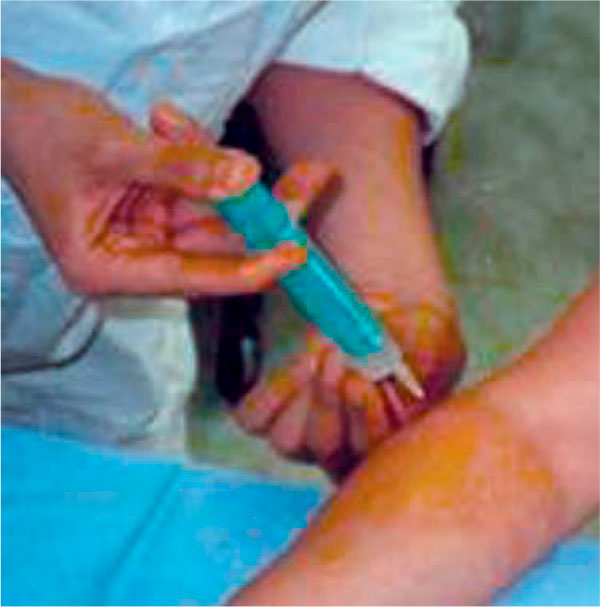
Рисунок 6. Методика перифокальных инъекций в мягкие ткани области локтевого эпикондилита
Было пролечено 10 пациентов (6 мужчин и 4 женщины) с эпикондилитами, средний возраст которых составил 47,6 ± 7,7 года. Пациентам в 1 болевую точку вводилось 2 мл Алфлутопа с 0,25%-ным раствором новокаина (рис. 6). Таких сеансов было проведено 5 с интервалами 2 раза в неделю. На графике (рис. 7) видно, что после лечения отметили значительное улучшение 3 человека, улучшение – 6 человек. Не почувствовал эффекта 1 больной.
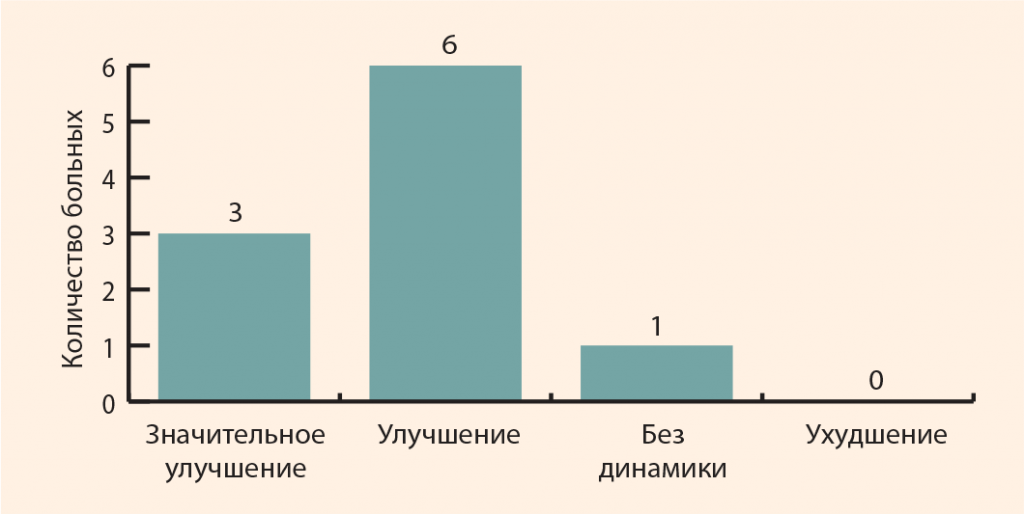
Рисунок 7. Результаты локальной терапии эпикондилитов
ЛЕЧЕНИЕ БОЛИ В СПИНЕ
Среди заболеваний, индуцирующих боль в области спины, патология мягких тканей составляет до 70% [22]. Главенствующую роль здесь играет рефлекторный болевой спазм паравертебральных мышц – дефанс мышц – «симптом вожжей». Нередкой причиной являются ЭТ спины: место прикрепления m. sacrospinaleis, переход длинной спинной мышцы в сухожилие, место прикрепления m. gluteus maximus, область перехода m. tensor fasciae latae в ягодичную фасцию, повреждения над- и межостных связок. Боли могут возникать в местах прикрепления мышц шеи к окципитальному гребню, ромбовидных мышц к внутреннему краю лопатки, косых мышц живота к гребням крыльев подвздошных костей. Данные патологии несложны в диагностике и легко поддаются локальной инъекционной терапии.
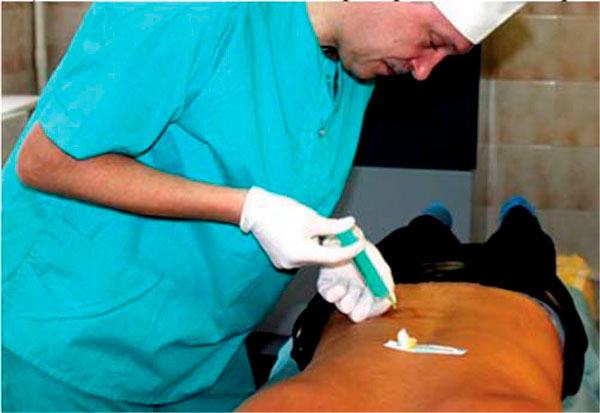
Рисунок 8. Методика перифокальных инъекций в область спины
Достоверно доказанное в двойном слепом плацебоконтролируемом исследовании уменьшение боли при вертеброневрологических синдромах после внутримышечного курса Алфлутопа (а именно: снижение боли в течение первого месяца, нарастающее действие в течение трех месяцев после отмены препарата, сохранение эффекта в течение шести месяцев) позволило использовать препарат локально при болях в спине [23].
Было пролечено 14 пациентов (9 мужчин и 5 женщин) с болью в спине в возрасте 48,4 ± 7,4 года. Больным на болевой стороне в 3–5 паравертебральных точек за 1 сеанс в сумме вводилось 2 мл Алфлутопа с 0,25%-ным раствором новокаина (рис. 8). Таких сеансов было проведено 5 с интервалами 2 раза в неделю. На графике (рис. 9) видно, что после лечения отметили значительное улучшение 6 человек и улучшение – 7 человек. Не почувствовал эффекта 1 больной. Отрицательных результатов не отметил никто.
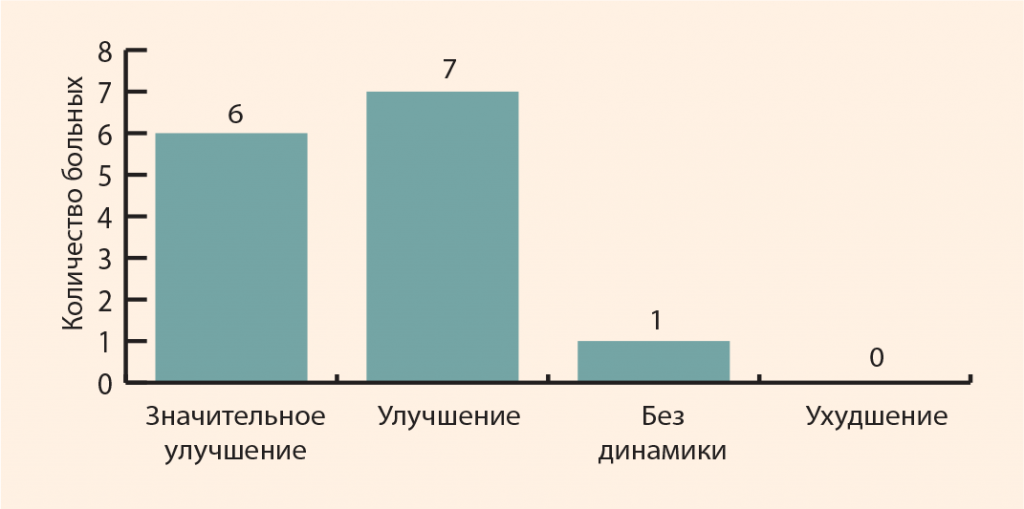
Рисунок 9. Результаты локальной терапии боли в спине
ЛЕЧЕНИЕ ТРОХАНТЕРИТОВ
ППАТ в бедренной области носят разнообразный характер и представлены в основном теномиозитами мышц бедра и их ЭТ, которые нередко протекают в безболевой форме и характеризуются щелчками при движении, слышимыми на расстоянии. Болевой синдром присутствует при энтезопатиях большого вертела бедренной кости с воспалительными явлениями в них [24].
При положении пациента на боку при слегка согнутой в тазобедренном и коленном суставах ноге, находящейся сверху, хорошо пальпируется выступающая сверху область большого вертела бедренной кости. Возникающий болевой синдром при этом расценивается как трохантерит. Варианты трохантеритов обычно включают в себя: ЭТ большого вертела и более редко встречаемый бурсит вертельной сумки. Причинами трохантерита являются врожденные или приобретенные нарушения строения таза или ног, большие механические нагрузки, травмы, переохлаждение, избыточная масса тела, особенно возникшая за короткий срок. Нередко причину установить не удается.
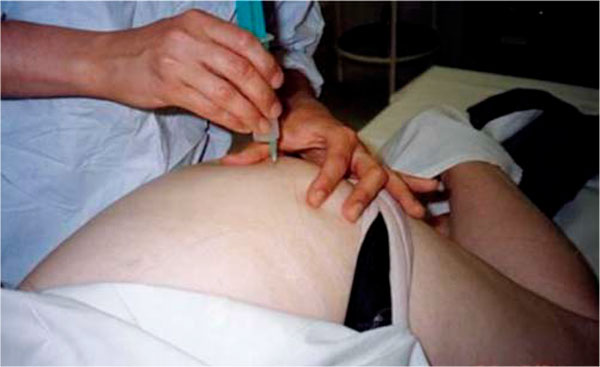
Рисунок 10. Методика перифокальных инъекций в область большого вертела бедренной кости
Энтезит большого вертела – частая причина болей в области бедра. Это заболевание осложняет течение коксартроза, но может протекать и без него. ЭТ проявляется болями, иррадиирущими по наружной поверхности бедра. Типичная жалоба больного – невозможность лежать, особенно спать на пораженном боку. Отмечается отчетливая локальная болезненность области большого вертела при пальпации, сохранность объема пассивных движений в тазобедренном суставе и боль при сопротивлении активному отведению бедра.
Было пролечено 13 пациентов (4 мужчины и 9 женщин) в возрасте 54,7 ± 8,9 года с клиникой трохантерита. Пациентам в 1–3 болевые точки мягких тканей в области большого вертела за 1 сеанс в сумме вводилось 2 мл Алфлутопа с 0,25%-ным раствором новокаина (рис. 10). Таких сеансов было проведено 5 с интервалами 2 раза в неделю. На графике (рис. 11) видно, что после лечения отметили значительное улучшение 8 человек и улучшение – 5 человек. Отсутствие динамики и отрицательных результатов никто не отметил.
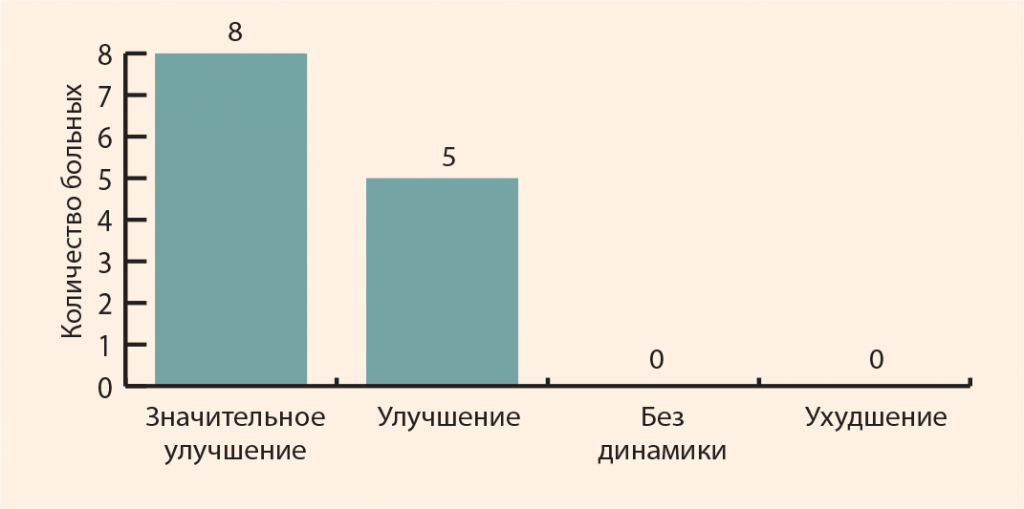
Рисунок 11. Результаты локальной терапии трохантеритов
ЛЕЧЕНИЕ АНЗЕРИНИТА КОЛЕННОГО СУСТАВА
Анзеринит является нередким вариантом ППАТ области коленного сустава. «Гусиная лапка» (pes anserinus) представляет собой место прикрепления к большеберцовой кости сухожилий портняжной (m. sartorius), тонкой (m. gracilis) и полусухожильной (m. semitendinosus) мышц.
Эта анатомическая область находится на 3–4 см ниже щели коленного сустава по медиальной его поверхности. Данная энтезопатия часто осложняет течение гонартроза. Возможно существование анзеринита при здоровом коленном суставе. Заболевание развивается часто у людей, которые много времени проводят на ногах. Развитию заболевания способствуют длительная ходьба, бег, игры и т. п.
Типичны жалобы больного на боль в данном месте. Больной указывает пальцем болезненную точку. Отмечается усиление боли при активном движении в колене. При пальпации определяется резкая локальная болезненность площадью 3–4 см2. Нередко симптомы энтезопатии «гусиной лапки» беспокоят пациента значительно больше, чем проявления собственно гонартроза [25, 26].
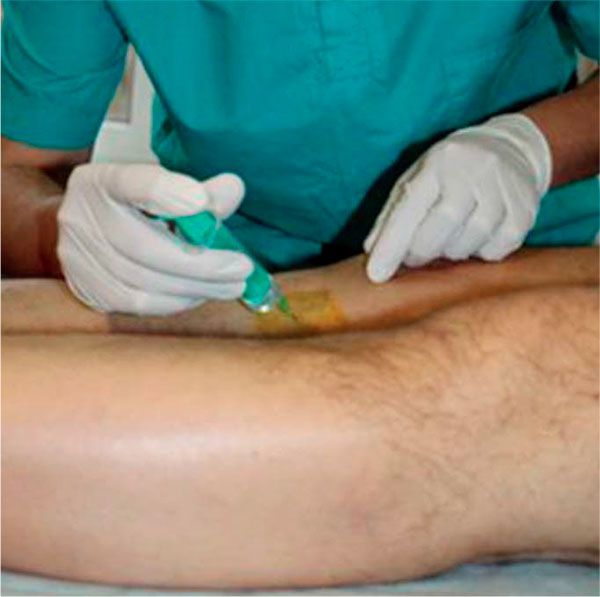
Рисунок 12. Методика перифокальных инъекций в область «гусиной лапки» коленного сустава
Было пролечено 9 пациентов (4 мужчины и 5 женщин) с клиникой анзеринита, средний возраст которых составил 53,4 ± 7,6 года. Пациентам в 1 точку мягких тканей «гусиной лапки», находящуюся ниже медиальной суставной щели на 3–4 см, за 1 сеанс в сумме вводилось 2 мл Алфлутопа с 0,25%-ным раствором новокаина (рис. 12). Было проведено 5 сеансов с интервалами 2 раза в неделю. На графике (рис. 13) видно, что после лечения отметили значительное улучшение 2 человека и улучшение – 6 человек. Один пациент не отметил динамики. Отрицательных результатов не отметил никто.
При выполнении перифокальных инъекций больные отмечали легкую болезненность, сопоставимую с внутримышечными инъекциями. Единично встречаемая кровоточивость из места инъекции легко устранялась прижатием ватного тампона на 1–2 минуты и не отражалась на дальнейшей терапии. Двое больных жаловались на легкое головокружение в течение 5–7 минут как реакцию на новокаин, что отмечалось и ранее. Двое больных с артериальной гипертензией отметили после 1-й инъекции повышение артериального давления, потребовавшее дополнительной медикаментозной коррекции и не повлиявшее на ход дальнейшего лечения. Один больной отмечал диспепсию после 2-й инъекции, сохранявшуюся до конца курса лечения.
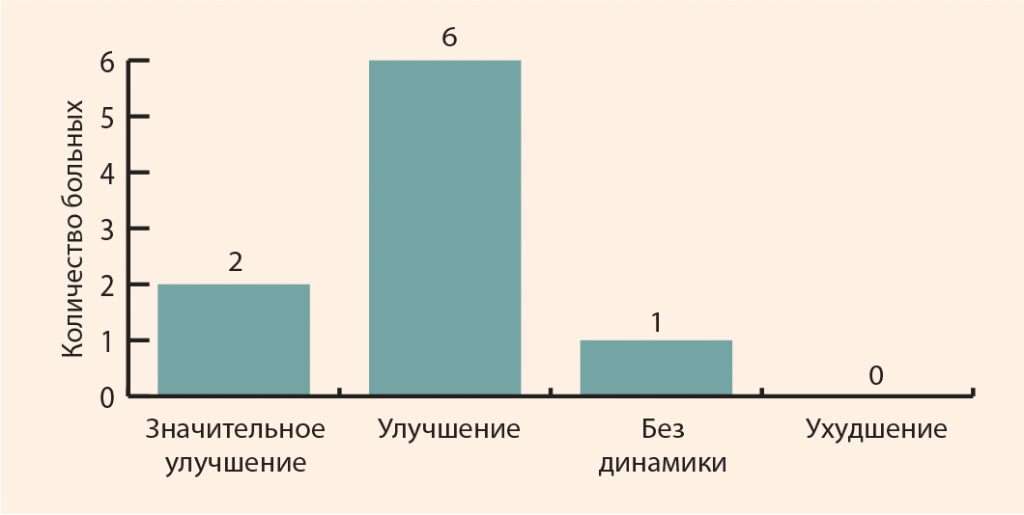
Рисунок 13. Результаты локальной терапии анзеринита коленного сустава