Резюме
Разрывы передней крестообразной связки (ПКС) коленного сустава являются актуальной проблемой спортивной медицины. Частота повреждений ПКС в популяции составляет 1 случай на 1000–10 000 ежегодно и увеличивается у лиц, занимающихся контактными видами спорта [1]. При полном разрыве ПКС требуется операция – реконструкция ПКС [2]. Возврат к прежнему спортивному уровню наблюдается только в 55% случаев, а у 45% спортсменов развивается персистирующий пателлофеморальный болевой синдром (ПФБС) [3]. ПФБС отмечается у всех спортсменов после реконструкции ПКС, и от эффективности программы реабилитации зависит, будет ли он устранен полностью или станет хроническим [4].
ПФБС – еще более частая проблема, чем разрывы ПКС, в общей популяции он встречается примерно в 25% случаев [5]. ПФБС является одной из наиболее распространенных патологий опорно-двигательного аппарата как у профессиональных спортсменов, так у спортсменов-любителей в возрасте старше 25 лет [6]. ПФБС характеризуется комплексом таких симптомов, как боль, отек и крепитация в области надколенника, выраженность которых зависит от механической нагрузки и двигательной активности.
Если биомеханика нижней конечности при ПФБС остается нарушенной, постепенно может развиваться остеоартрит (ОА) коленного сустава, прогрессирование которого, приводит к необходимости эндопротезирования. Высокая распространенность и социальная значимость ОА диктуют необходимость комплексного подхода к лечению, направленного на уменьшение боли, улучшение функционального состояния суставов, предотвращение/замедление прогрессирования болезни и снижение риска инвалидизации. Современные клинические рекомендации по ведению больных ОА предусматривают использование нефармакологических и медикаментозных методов терапии.
Исследование функциональных возможностей нижней конечности имеет большое значение для разработки и корректного выбора немедикаментозных методов лечения. Так, стабилометрия дает возможность объективно оценивать функциональные возможности нижних конечностей. Показано, что проприоцептивная информация играет значительную роль в поддержании статокинетической устойчивости [7]. Сенсомоторная система включает все сенсорные, моторные, а также центральные интеграционные и исполнительные компоненты, вовлеченные в поддержание функциональной стабильности сустава [8]. Статокинетическая устойчивость обеспечивается центральной нервной системой за счет получения афферентации по трем основным путям: проприоцептивному, визуальному и вестибулярному [9].
Исследование статокинетической устойчивости выявило ухудшение показателей у пациентов после травм различных суставов и их лечения [10–17], а также при ОА голеностопного, коленного и тазобедренного суставов [18]. Обнаружена связь между нарушением стабильности коленного сустава в сагиттальной плоскости и двусторонним нарушением статокинетической устойчивости у спортсменов с изолированным давним повреждением ПКС [19]. При сравнении двух групп пациентов с дефицитом ПКС со значительно выраженной нестабильностью и отсутствием симптомов отмечена закономерность: пациенты с выраженным дефицитом ПКС имели более низкие проприоцептивные возможности (по данным стабилометрии) по сравнению с лицами, не имевшими симптомов [20]. Статокинетическую устойчивость в сагиттальной плоскости оценивали у пациентов с хронической недостаточностью ПКС и у лиц контрольной группы [21]. Установлены значительный дефицит устойчивости (при стоянии на одной ноге) в группе пациентов с хронической недостаточностью ПКС по сравнению с контролем, а также значительная его вариабельность внутри группы пациентов с хронической недостаточностью ПКС. Этих пациентов обследовали до начала курса реабилитации (через 3–6 мес после травмы) [17]. При этом обнаружено значительное нарушение баланса при стоянии на обеих ногах по сравнению с контролем. Нормальные показатели при стоянии на поврежденной ноге отмечались после 12 и 36 мес реабилитации. Таким образом, была показана возможность восстановления статокинетической устойчивости при консервативном лечении полного разрыва ПКС.
В медикаментозной терапии особое место занимают симптоматические средства замедленного действия (Symptomatic Slow Acting Drugs for Osteoarthritis, SYSADOA), которые считаются базисными, поскольку имеются четкие доказательства их симптоматического, противовоспалительного и структурно-модифицирующего действия при ОА различных локализаций [22, 23]. При травматическом повреждении сустава для получения более быстрого анальгетического эффекта и повышения биодоступности эти препараты могут назначаться парентерально.
Один из таких препаратов – Алфлутоп1(1Biotehnos (Румыния); стандартизированный стерильный биоактивный концентрат из четырех видов мелких морских рыб, БКММР), успешно применяемый в ревматологической практике около 30 лет. Первоначально считалось, что препарат имеет антигиалуронидазную активность и стимулирует синтез эндогенной гиалуроновой кислоты. Позднее было показано, что Алфлутоп оказывает многокомпонентное действие: позитивно влияет на метаболизм хондроцитов и замедляет апоптоз; подавляет активность некоторых провоспалительных медиаторов, включая интерлейкин (ИЛ) 6, ИЛ8 и ИЛ1β и др.; замедляет деградацию экстрацеллюлярного матрикса, опосредованную матриксными металлопротеиназами (ММП), включая ADAMTS4, ММП13, ММП3, и ангиогенез; воздействует на сосудистый эндотелиальный фактор роста; стимулирует хондрогенез за счет влияния на внеклеточное высвобождение трансформирующего фактора роста β [24]. Описан также антиоксидантный эффект препарата, связанный с увеличением активности каталазы и уменьшением уровня внутриклеточного супероксид анион/пероксида водорода, что имеет значение для метаболизма митохондрий [24].
Этот препарат широко используется для лечения ОА, имеет хорошую доказательную базу, включающую двойные слепые рандомизированные клинические исследования, подтвердившие его анальгетический, противовоспалительный и структурно-модифицирующий эффект [25, 26].
Материалы и методы исследования
Пациенты и методы. В исследовании участвовали 40 мужчин (средний возраст – 24±6,6 года, масса тела – 67,4±11,5 кг), занимающихся игровыми видами спорта, перенесших реконструкцию ПКС. Больных включали в исследование через 2 мес после операции.Критерии включения: передняя боль в коленном суставе, положительный тест Фалкерсона, явления хондромаляции фасеток надколенника 1–2-й степени по данным магнитнорезонансной томографии.
Оценивалась боль по числовой рейтинговой шкале – ЧРШ (от 0 до 10, где 10 – максимальная выраженность боли); функциональное состояние коленного сустава по шкале Kujala (в баллах от 0 до 100); статокинетическая устойчивость с помощью стабилометрического исследования на стабилоплатформе «Траст-М СТАБИЛО» («Нейрокор», Россия). Исследование проводили в положении обследуемого в европейской стойке. При проведении теста Ромберга основными показателями были: площадь общего центра давления (ОЦД, в мм2), скорость смещения ОЦД (в мм/c).
Пациенты методом случайной выборки были разделены на две группы. В контрольной группе (n=20) использовалась специальная методика реабилитации после реконструкции ПКС [27]. В основной группе (n=20) наряду с аналогичной методикой реабилитации пациенты получали курс внутримышечных инъекций (по 1 мл, № 20) препарата Алфлутоп. Длительность восстановительных мероприятий – 1 мес. Состояние спортсменов оценивали до и после курса реабилитации.
Исследование одобрено этическим комитетом ГАУЗ «Московский научно-практический центр медицинской реабилитации, восстановительной и спортивной медицины Департамента здравоохранения города Москвы». Все пациенты подписали информированное согласие на участие в исследовании.
Статистические методы включали оценку полученных данных на нормальность распределения, парный критерий Стьюдента. Использовали программу Microsoft Excel. Изменения считали значимыми при уровне р<0,05.
Результаты исследования
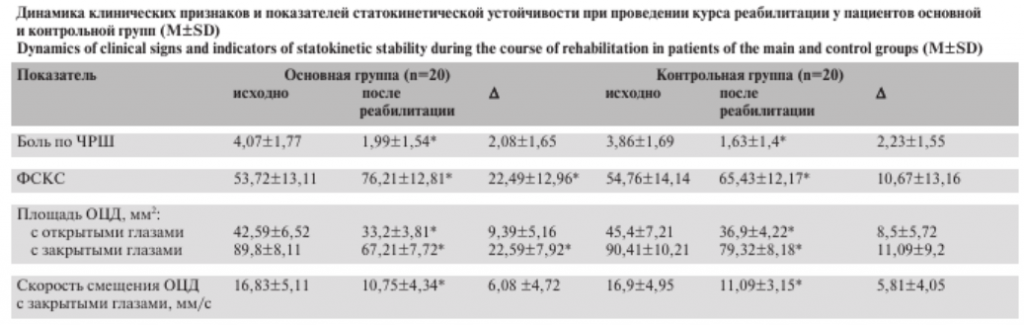
Как показали данные исследования, через 1 мес после начала восстановительных мероприятий в обеих группах отмечены значимое уменьшение интенсивности боли и улучшение функционального состояния коленного сустава по опроснику Kujala (см. таблицу).
Исследование показателей статокинетической устойчивости выявило следующие закономерности. После курса реабилитации в обеих группах при стоянии с открытыми глазами отмечались уменьшение площади ОЦД (р<0,05) и улучшение статокинетической устойчивости, а при стоянии с закрытыми глазами – уменьшение площади ОЦД (р<0,05). При этом разница результатов до и после курса реабилитации в основной группе была значимо большей по сравнению с таковой в контроле (р<0,05). Скорость смещения ОЦД с открытыми глазами в обеих группах существенно не менялась: при стоянии с закрытыми глазами выявлена ее положительная динамика после курса реабилитации (р<0,05; см. таблицу).
Обсуждение результатов
После курса восстановительного лечения у спортсменов обеих групп, перенесших реконструкцию ПКС, выявлена положительная динамика: уменьшился болевой синдром, улучшились функция коленного сустава по опроснику Kujala и статокинетическая устойчивость в позе Ромберга. В группе контроля использовалась специальная лечебная гимнастика, курсовое применение которой уменьшило интенсивность боли по ЧРШ и улучшило функцию коленного сустава, повысило статокинетическую устойчивость по площади ОЦД с закрытыми и открытыми глазами и скорости смещения ОЦД с закрытыми глазами. При этом результаты обследования по опроснику Kujala, отражающие состояние коленного сустава, включают оценку спортивной активности. Разница счета по опроснику Kujala до и после курса комплексного лечения была выше в основной группе, что свидетельствовало о лучшем уровне восстановления функции коленного сустава у этих пациентов. В основной группе после курса реабилитации показатели площади ОЦД с закрытыми глазами были значимо лучше, чем в контрольной группе. Статокинетическая устойчивость с закрытыми глазами (с исключением зрительного анализатора) в большей степени отражает проприоцептивные возможности опорно-двигательного аппарата. Улучшение ее показателей у пациентов основной группы, очевидно, было связано с увеличением функциональных способностей коленного сустава.Применение Алфлутопа у больных основной группы вызвало значимое улучшение функции коленного сустава по сравнению с показателями в контрольной группе, что, возможно, связано с анальгетическим и противовоспалительным действием этого препарата, а улучшение показателей площади ОЦД с закрытыми глазами – с оптимизацией функции коленного сустава. Интересно, что на фоне применения Алфлутопа увеличились функциональные способности и двигательные функциональные возможности спортсменов основной группы.
Подтверждением противовоспалительного действия оригинального БКММР служат результаты исследования репарации посттравматического повреждения сухожилий у 60 половозрелых аутбредных белых крыс (30 особей получали Алфлутоп внутримышечно ежедневно по 0,05 мл в течение 30 дней, еще 30 крыс вошли в контрольную группу) [28]. Выявлено позитивное влияние препарата на репаративные процессы в сухожилии икроножной мышцы крыс.
Развитие посттравматического ОА – самое частое осложнение любой травмы сустава. Своевременное и правильное применение комплекса реабилитационных и медикаментозных методов может иметь большое значение для профилактики ОА у таких больных, однако требуются дальнейшие проспективные наблюдения для выработки правильной стратегии их ведения.